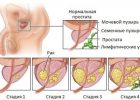
Нефротический синдром — экскреция с мочой более 3 г белка в день в результате патологии почечных клубочков. Он больше распространен у детей и имеет как первичные, так и вторичные причины. Диагностика нефротического синдрома основывается на измерении отношения белок/креатинин мочи или суточного белка мочи; основные причины диагностируются на основании анамнеза, физикального обследования и биопсии почек. Лечение нефротического синдрома и прогноз, зависят от причины.
Нефротический синдром — причины возникновения у детей
Нефротический синдром встречается в любом возрасте, но более распространен у детей, главным образом в 1,5-4 года. В младшем возрасте мальчики чаще болеют, чем девочки; в старшем возрасте и мальчики и девочки болеют одинаково часто. Причины нефротического синдрома различны в разных возрастах. Самые распространенные первичные причины:
- болезнь минимальных изменений,
- фокальный сегментарный гломерулосклероз,
- мембранозная нефропатия.
Вторичные причины ответственны менее чем за 10 % случаев в детском возрасте, но более чем за 50 % во взрослом, обычно это диабетическая нефропатия и преэклампсия. Амилоидоз — нераспознанная причина 4 % всех случаев НС.
Протеинурия возникает из-за изменений эндотелиальных клеток капилляров, базальной мембраны клубочков, или подоцитов, которые в норме фильтруют белок плазмы крови селективно по размеру и весу. Механизм повреждения этих структур не известен при первичной патологии клубочков, но предполагают, что Т-лимфоциты чрезмерно продуцируют циркулирующий фактор проницаемости или угнетают продукцию ингибирующего фактора проницаемости в ответ на неопределенные иммуногены и цитокины. В результате происходит потеря с мочой макромолекулярных белков, прежде всего:
- альбумина,
- опсонинов,
- иммуноглобулинов,
- эритропоэтина,
- трансферрина,
- гормонсвязывающих белков,
- антитромбина, при патологиях, вызывающих неселективную протеинурию.
В результате у пациентов с нефротическим синдромом развиваются периферические отеки, асцит, выпоты и повышается риск инфекционных осложнений, анемия; нарушения функции щитовидной железы; тромбоэмболия (у 5 % детей и 40 % взрослых). Тромбоэмболия может развиться не только из-за потери с мочой антитромбина, но также и из-за увеличенного печеночного синтеза факторов свертывающей системы крови, нарушения функции тромбоцитов и повышения вязкости на фоне гиповолемии. Хронические осложнения нефротического синдрома включают истощение у детей, коронарную патологию у взрослых, хроническую почечную недостаточность и болезни костной ткани. Истощение может напоминать квашиоркор, включая ломкость волос и ногтей, облысение и замедление роста. Коронарная патология развивается, поскольку НС вызывает гиперлипидемию, артериальную гипертензию, и гиперкоагуляцию. Патология кости развивается из-за дефицита витамина D и применения глюкокортикоидов. Другие хронические осложнения включают гипотиреоз в результате потери тироглобулина и проксимальной канальцевой дисфункции, вызывающей:
- глюкозурию,
- аминоацидурию,
- потерю калия,
- фосфатурию,
- почечный канальцевый ацидоз.
Почечная недостаточность редко является первичным проявлением, но может развиться на поздней стадии болезни. Однако у пациентов с нефротическим синдромом, в результате вторичных причин часто имеется почечная недостаточность исходно или вскоре после манифестации.
Симптомы нефротического синдрома
Первичные симптомы включают анорексию, недомогание и пенистую мочу, вызванную высокими концентрациями белка. Задержка жидкости может вызывать одышку, дискомфорт в груди, артралгию или боли в животе. Отеки могут маскировать симптомы мышечного истощения и вызывать появление параллельных белых линий в ногтевом ложе.
Остальные симптомы обусловлены многочисленными осложнениями НС.
Диагностика при нефротическом синдроме
Диагноз подозревают у больных с отеками и протеинурией, выявленной при анализе мочи и подтвержденной суточным измерением экскретируемого с мочой белка. Этиологию можно предположить на основании анамнеза ; когда причина не ясна, показаны серологические тесты и биопсия почек.
Содержание 3 г белка в суточной моче имеет диагностическое значение. Отношение белок/креатинин в случайном анализе мочи соответствует количеству выделенного белка, приведенного к 1,73 м площади поверхности тела в суточном количестве мочи. Использование отношения белка к креатинину в образце мочи может быть менее надежным, когда экскреция креатинина чрезвычайно высокая или низкая и при нарушениях, когда протеинурия может изменяться ежедневно.
Помимо протеинурии, анализ мочи может показать наличие эритроцитов и цилиндров. Липидурия — наличие свободного жира в канальцевых клетках, в цилиндрах или в виде свободных шариков — присутствует исходно, если причиной НС является патология клубочков. Холестерин в моче может быть обнаружен при простой микроскопии и имеет вид «мальтийского пересечения» под поляризованным светом; окрашивание Суданом должно использоваться для выявления триглицеридов. Лейкоциты присутствуют в значительном количестве при экссудативных заболеваниях и СКВ.
Дополнительные тесты помогают охарактеризовать тяжесть и осложнения патологии. Концентрации креатинина и азота изменяются в зависимости от степени нарушения почечной функции. Содержание альбумина часто менее 25 г/л. Содержание общего холестерина и триглицеридов обычно повышается. Нет необходимости в рутинном исследовании уровней а- и у-глобулинов, иммуноглобулинов, гормонсвязывающих белков, церулоплазмина, трансферрина и компонентов комплемента, но они могут также быть низкими.
У взрослых биопсия почек показана для диагностики основной причины идиопатических НС. Идиопатический нефротический синдром у детей наиболее вероятно представляет болезнь минимальных изменений и обычно диагностируется без биопсии, кроме случаев, когда нет реакции на пробный курс глюкокортикоидов. Специфические морфологические черты обсуждены ниже в разделах заболеваний.
Нефротический синдром: прогноз
Прогноз определяется причиной НС. Полная ремиссия может быть как спонтанной, так и на фоне лечения нефротического синдрома. Прогноз в целом благоприятен при заболеваниях, чувствительных к глюкокортикоидам. В любом случае, прогноз может ухудшиться при инфекционных осложнениях; артериальной гипертензии; выраженной азотемии; гематурии или тромбозах мозговых, легочных, периферических или почечных вен. Частота рецидивов высока у пациентов после трансплантации почки по поводу центрального сегментарного гломерулосклероза, СКВ, lgA-нефропатии и мембрано-пролиферативного гломерулонефрита.
Нефротический синдром: лечение
Специфическое лечение нефротического синдрома, рассмотрено ниже, в разделах заболеваний. Поддерживающая терапия включает лечение вторичных причин, когда они имеются, и диетические ограничения, гипотензивные средства и меры предотвращения осложнений. Редко тяжелый НС требует нефрэктомии из-за персистирующей гипоальбуминемии. Лечение нефротического синдрома и основных причин, может включать своевременную терапию инфекций, гипосенсибилизацию и препараты базисной терапии. Указанные меры могут излечить НС в определенных случаях. Ограничение диетического белка больше не рекомендуется из-за недоказанного эффекта на прогрессию заболевания. Однако употребление насыщенных жиров и холестерина должно быть ограничено, а ограничение приема натрия рекомендуется для коррекции отеков. Ингибиторы АПФ показаны для уменьшения системного и внутриклубочкового артериального давления и протеинурии. У больных с умеренной и тяжелой почечной недостаточностью они могут вызвать или усилить гиперкалиемию. Петлевые диуретики обычно требуются для коррекции отеков, но могут усугубить уже имеющуюся почечную недостаточность и гиповолемию, вязкость крови и гиперкоагуляцию. Антикоагулянты показаны при тромбоэмболических осложнениях, но очень немногочисленные данные имеются в поддержку их использования в качестве первичной профилактики. Статины показаны при гиперлипидемии. Все пациенты должны получить пневмококковую вакцину; использование пенициллина как профилактического средства спорно.
Врожденные нефротические синдромы
Врожденные нефротические синдромы включают диффузный мезангиальный склероз и финский тип НС.
Диффузный мезангиальный склероз — заболевание редкое. Данных в пользу наследования заболевания нет. Пациенту с тяжелой протеинурией может потребоваться двусторонняя нефрэктомия из-за выраженной гипоальбуминемии; диализ следует начинать на ранних сроках заболевания для коррекции нутритивного дефицита и облегчения качества жизни. Болезнь обычно рецидивирует в почечном трансплантате.
Финский тип нефротического синдрома — аутосомно-рецессивное заболевание, которое встречается у 1 из 8200 финских новорожденных. Оно вызвано мутацией в гене NPHS1, который кодирует синтез подоцитарного белка щелевой диафрагмы. Финский тип НС является быстро прогрессирующим и обычно в течение 1 года применяют диализ. Большинство пациентов умирает в течение года, но некоторые поддерживаются нутритивно до развития почечной недостаточности, они нуждаются в диализе или трансплантации.
Другие редкие врожденные нефротические синдромы в настоящее время генетически охарактеризованы. Они включают резистентный к глюкокортикоидам НС, семейный фокальный сегментарный гломерулосклероз и синдром Denys-Drash.
Данная статья размещена исключительно в общих познавательных целях посетителей и не является научным материалом, универсальной инструкцией или профессиональным медицинским советом, и не заменяет приём доктора. За диагностикой и лечением обращайтесь только к квалифицированным врачам, в государственных больницах и частных клиниках.